Em 24 de abril de 2026, durante a 636ª Reunião Ordinária da Diretoria Colegiada, a Agência Nacional de Saúde Suplementar deliberou pela não incorporação ao Rol de Procedimentos e Eventos em Saúde da combinação talazoparibe (Talzenna®) + enzalutamida (Xtandi®) — primeira linha em câncer de próstata metastático resistente à castração com mutação HRR. A pauta foi conduzida pela diretoria reguladora de produtos (DIPRO), com a presença do diretor-presidente Wadih Damous e dos diretores Eliane Medeiros, Lenise Secchin, Carla Soares e Jorge Aquino. A decisão administrativa, contudo, não autoriza a recusa contratual: a Lei 14.454/2022 e a jurisprudência consolidada do STJ asseguram cobertura quando há prescrição médica fundamentada, registro ANVISA presente e evidência científica robusta — todos os três critérios estão satisfeitos.
A deliberação encerra processo administrativo de mais de quatro meses, iniciado pela 47ª Reunião Técnica da COSAÚDE em 28 de janeiro de 2026, passando pela Consulta Pública nº 167/2026 (encerrada em 1º de março de 2026) e culminando na decisão colegiada do dia 24 de abril. A não incorporação ao Rol é juridicamente um ato regulatório — diz respeito ao que a ANS considera devido como cobertura mínima geral, não ao que a operadora deve ao paciente individual no caso concreto. São realidades distintas após a Lei 14.454/2022.
Belisário Maciel Advogados acompanha cada deliberação da DICOL relacionada a oncologia e mantém o cluster jurídico mais aprofundado do mercado brasileiro em direito oncológico — com mais de 47 análises técnicas publicadas, cobrindo medicamentos de alto custo (Keytruda, Opdivo, Herceptin, Enhertu, Tagrisso, Lynparza, Verzenio, Ibrance, Trodelvy, Yervoy, Braftovi, Tecentriq, Kadcyla), procedimentos (radioterapia IMRT/SBRT, PET-CT, cirurgia oncológica, transplante de medula, CAR-T) e teses jurídicas das operadoras (custo desproporcional, off-label, tratamento experimental, sem registro ANVISA). A análise abaixo mapeia a decisão, o medicamento, a evidência clínica e a tese jurídica que sustenta a cobertura para o paciente.
Linha do tempo do processo administrativo na ANS
A decisão de 24/04/2026 é o último ato de um processo administrativo iniciado em janeiro. Conhecer cada fase é importante para compreender o tipo de revisão que cabe — administrativa (recurso à ANS, mandado de segurança contra ato administrativo) ou contratual (ação contra a operadora com fundamento na Lei 14.454/2022).
- 28/jan/2026 — Avaliação técnica COSAÚDE. A 47ª Reunião Técnica da Comissão de Atualização do Rol avaliou a proposta de incorporação. Foi nesse momento que se elaborou o Relatório Técnico nº 47 (UAT 190), com análise de evidência clínica, custo-efetividade e impacto orçamentário.
- fev–1º/mar/2026 — Consulta Pública nº 167/2026. A ANS abriu consulta pública para receber contribuições da sociedade. Sociedades médicas, fabricante (Pfizer), associações de pacientes, advogados especializados e a Sociedade Brasileira de Urologia contribuíram tecnicamente.
- mar/2026 — Análise das contribuições. A área técnica analisou as contribuições recebidas, consolidou parecer e enviou recomendação à diretoria para deliberação colegiada.
- 24/abr/2026 — Decisão DICOL. Na 636ª Reunião Ordinária da Diretoria Colegiada, deliberação pela não incorporação. Decisão é publicada no Diário Oficial da União e produz efeitos administrativos a partir da publicação.
- Após decisão — Recurso administrativo. Cabe recurso ao próprio órgão (Lei 9.784/99) e, posteriormente, ação anulatória na Justiça Federal por interessados na incorporação. Para pacientes individuais, contudo, a via mais célere é a ação contra a operadora com base na Lei 14.454/2022.
- Médio prazo — Possibilidade de reincorporação. A não incorporação não é definitiva — nova análise é cabível com novos estudos, novas avaliações de custo-efetividade ou em ciclos posteriores de atualização. Histórico mostra reincorporações em ciclos de 12 a 24 meses.
Talzenna + Xtandi — o que é e como age
A combinação talazoparibe (Talzenna®) + enzalutamida (Xtandi®) integra dois mecanismos farmacológicos distintos contra o câncer de próstata avançado.
O talazoparibe é um inibidor da PARP (poli ADP-ribose polimerase), enzima envolvida no reparo de DNA. Em pacientes com mutações nos genes de reparo por recombinação homóloga (HRR — BRCA1, BRCA2, ATM, CHEK2, PALB2, FANCA, MLH1, RAD51 e outros), o bloqueio da PARP impede que as células tumorais reparem suas próprias quebras de DNA, levando à morte celular por letalidade sintética. É comercializado como Talzenna® pela Pfizer.
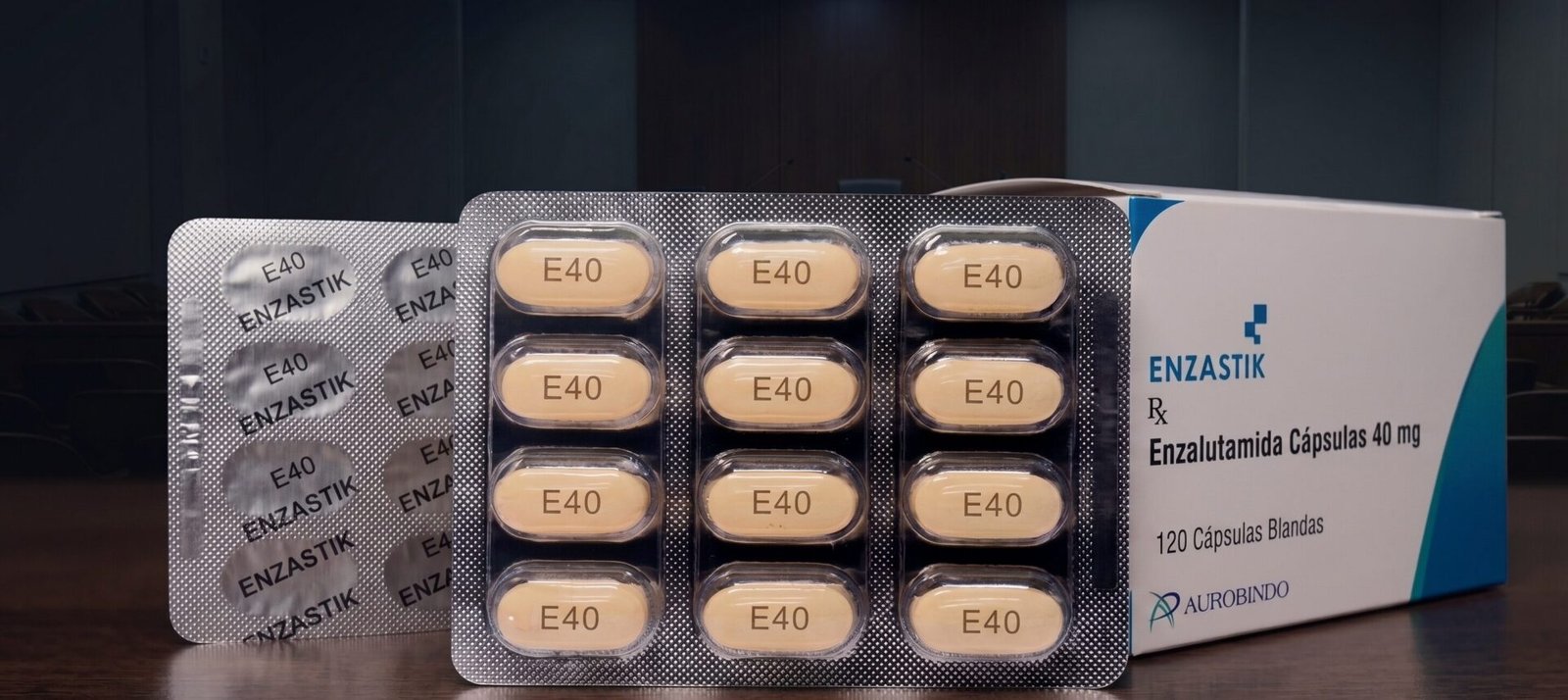
A enzalutamida é um inibidor da via androgênica de segunda geração (ARPI — Androgen Receptor Pathway Inhibitor). Bloqueia a ação dos androgênios sobre o tumor de próstata em três pontos: ligação do androgênio ao receptor, translocação do receptor para o núcleo e ligação do complexo ao DNA. É comercializada como Xtandi® pela Astellas/Pfizer e também há versão genérica disponível no Brasil (Enzastik®, Aurobindo). Cápsulas orais de 40 mg, com posologia padrão de 160 mg/dia (4 cápsulas).
A combinação aproveita um efeito sinérgico: a inibição androgênica induz vulnerabilidade ao reparo de DNA, intensificando o efeito do PARP-inibidor independentemente da presença de mutação HRR — embora o ganho seja maior em pacientes HRR-mutados. Ambos são medicamentos orais, enquadrando-se na cobertura obrigatória de quimioterápicos antineoplásicos orais imposta pela Lei 12.880/2013 aos planos de saúde brasileiros.
Indicação clínica e perfil do paciente HRR
A combinação foi aprovada para o tratamento de câncer de próstata metastático resistente à castração (mCRPC) — situação em que o tumor já se espalhou para outros órgãos (geralmente ossos, linfonodos, fígado ou pulmões) e progrediu apesar do bloqueio androgênico inicial (cirurgia de orquiectomia ou medicação de bloqueio). Nesta fase avançada da doença, a expectativa de vida sem tratamento adequado é geralmente inferior a 24-36 meses.
Aproximadamente 25% dos pacientes com mCRPC apresentam mutações HRR, sendo as mais frequentes:
- BRCA2 — a mais comum (~10-12% dos casos), associada a doença mais agressiva e melhor resposta a PARP-inibidores.
- BRCA1 — menos frequente (~1-2%) mas com mesmo perfil de resposta.
- ATM — segunda mais comum (~5-7%), com resposta menor mas ainda relevante.
- CHEK2, PALB2, RAD51, FANCA — frequências menores, resposta variável.
A identificação dessas mutações é feita por painel NGS (Next-Generation Sequencing) em tecido tumoral ou em sangue periférico (ctDNA — DNA tumoral circulante). A cobertura do painel NGS pelo plano também é obrigatória quando há indicação para terapia-alvo, conforme entendimento consolidado da jurisprudência.
Eficácia clínica — estudo TALAPRO-2
O estudo TALAPRO-2 (NCT03395197) é um ensaio clínico de fase 3, randomizado, duplo-cego, controlado por placebo, conduzido em 1.035 pacientes com câncer de próstata metastático resistente à castração em centros nos Estados Unidos, Canadá, Europa, América do Sul e Ásia-Pacífico. Foi o estudo pivotal para aprovação da combinação no mundo inteiro.
Os pacientes foram divididos em duas coortes: a coorte 1 (n=805, todos os pacientes mCRPC, independentemente de mutação) e a coorte 2 (n=399, somente pacientes com mutação HRR confirmada). Em ambas, os pacientes foram randomizados 1:1 entre combinação talazoparibe 0,5 mg/dia + enzalutamida 160 mg/dia versus placebo + enzalutamida 160 mg/dia.
| Desfecho | Combinação (Talzenna + Xtandi) | Monoterapia (Xtandi + placebo) | Significância |
|---|---|---|---|
| Sobrevida global mediana — HRR-mutados | 45,1 meses | 31,1 meses | HR 0,62 (redução de 38% no risco de morte) |
| Sobrevida global mediana — não selecionados | 45,8 meses | 37,0 meses | HR 0,80 (ganho de ~9 meses) |
| Sobrevida livre de progressão (PFS) — HRR-mutados | 27,9 meses | 16,4 meses | HR 0,46 (redução de 54% no risco de progressão) |
| Taxa de resposta objetiva (ORR) | 67,1% | 40,1% | +27 pontos percentuais |
| Tempo até quimioterapia citotóxica | ~37 meses | ~19 meses | Praticamente o dobro |
Os resultados foram apresentados no ASCO GU 2024 (American Society of Clinical Oncology — Genitourinary Cancers Symposium) e publicados em revistas de alto impacto, incluindo The Lancet. Em todas as métricas relevantes — sobrevida global, sobrevida livre de progressão, taxa de resposta objetiva, qualidade de vida e tempo até a quimioterapia citotóxica — a combinação demonstrou benefício estatisticamente significativo e clinicamente relevante.
O ganho de 14 meses de sobrevida em pacientes HRR-mutados é um dos maiores benefícios já demonstrados em estudos de mCRPC. Para contextualizar: cada mês de sobrevida em câncer metastático custou décadas de pesquisa; um ganho de mais de um ano configura mudança de patamar terapêutico.
Status regulatório — ANVISA, FDA e EMA
A combinação Talzenna® + Xtandi® possui aprovação regulatória sólida em todas as principais agências do mundo. O FDA (Estados Unidos) aprovou a combinação em 20 de junho de 2023 para mCRPC com mutação HRR; em 2025, a FDA expandiu a indicação após nova análise dos dados TALAPRO-2 com seguimento mais longo. A EMA (União Europeia) aprovou em 2024 com a mesma indicação. A ANVISA aprovou no Brasil — o registro vigente é o ponto-chave para a aplicação do Tema 990 do STJ a contrario sensu: medicamento com registro ANVISA é cobertura obrigatória pelos planos. No total, a combinação está aprovada e em uso clínico em mais de 35 países.
O registro ANVISA é especialmente relevante porque afasta um dos argumentos clássicos das operadoras — “tratamento experimental” ou “sem registro” — e ativa a aplicação direta da Súmula 102 do TJSP, que encerra de modo definitivo as teses de “experimental”, “off-label” e “fora do rol”.
Por que a ANS recusou e por que isso não vincula a operadora
O Relatório Técnico nº 47 da COSAÚDE (UAT 190) avaliou a proposta sob critérios técnicos que combinam evidência científica e análise de custo-efetividade. Embora o detalhamento integral do parecer envolva metodologia complexa, é possível identificar duas categorias de razões prováveis para a não incorporação. Razões de natureza econômica: a combinação tem custo elevado (em torno de R$ 35.000 a R$ 50.000 por mês considerando os dois medicamentos) e o impacto orçamentário no sistema é significativo, sobretudo se considerada a população elegível (~25% dos pacientes mCRPC com mutação HRR identificada). Razões de natureza técnica: questionamentos sobre o desenho do estudo, robustez do benefício em subgrupos, comparabilidade frente a alternativas terapêuticas (enzalutamida em monoterapia, abiraterona, docetaxel), incerteza sobre durabilidade do benefício após o seguimento atual.
É importante destacar, contudo, que a recusa administrativa de incorporação não tem efeito vinculante sobre a obrigação contratual da operadora frente ao paciente individual. Após a Lei 14.454/2022, a Lei dos Planos de Saúde foi alterada para estabelecer que o Rol é referência básica (não taxativo), e a cobertura é obrigatória quando satisfeitos critérios objetivos previstos no §13 do art. 10 da Lei 9.656/98:
- existência de comprovação da eficácia, à luz das ciências da saúde, baseada em evidências científicas e plano terapêutico;
- recomendações pela CONITEC ou aprovação por órgão de avaliação de tecnologias em saúde de renome internacional;
- recomendação por mais de um órgão de avaliação de tecnologias em saúde nacional ou internacional.
Os três critérios estão satisfeitos pela combinação Talzenna + Xtandi: estudo TALAPRO-2 (fase 3, 1.035 pacientes, sobrevida global estatisticamente significativa) atende ao primeiro; aprovações da FDA e EMA atendem aos segundo e terceiro. A recusa da ANS é, juridicamente, irrelevante para o caso individual.
Tese jurídica: precedentes que sustentam a cobertura
A jurisprudência consolidada do STJ e do TJSP afasta os argumentos administrativos de “fora do rol” e “experimental” quando há registro ANVISA, prescrição médica fundamentada e evidência científica robusta. Os precedentes abaixo sustentam a tese de cobertura para a combinação Talzenna + Xtandi em paciente com câncer de próstata metastático resistente à castração e mutação HRR.
- Tema 990/STJ (REsp 1.712.163/SP, Min. Moura Ribeiro, 24/11/2017). Aplicação a contrario sensu — medicamento com registro ANVISA tem cobertura obrigatória pelos planos. Talzenna e Xtandi têm registro ANVISA.
- REsp 1.279.241/SP (Min. Sanseverino, 4ª Turma, 2014). Restrição do art. 10, I, da Lei 9.656/98 só se aplica quando há tratamento convencional eficaz disponível.
- REsp 1.769.557/CE (Min. Nancy Andrighi, 3ª Turma). A escolha terapêutica é prerrogativa do médico assistente, não da operadora ou de comissão técnica administrativa.
- Lei 14.454/2022. Tornou o Rol da ANS exemplificativo. Os §§ 12 e 13 do art. 10 da Lei 9.656/98 criam camadas de proteção para cobertura fora do Rol — todas satisfeitas pela combinação.
- REsp 2.210.091/SP (Min. Nancy Andrighi, 3ª Turma, jun/2025). As duas Turmas da 2ª Seção do STJ têm posição unânime em oncologia: a recusa de cobertura é abusiva.
- AREsp 3.066.406/STJ (Min. Marco Buzzi, fev/2026). Medicamentos oncológicos estão fora do sistema do Rol da ANS — discussão sobre taxatividade é juridicamente irrelevante em oncologia.
- Súmula 102/TJSP encerra os argumentos “experimental”, “off-label” e “fora do rol” em comando interpretativo único: havendo prescrição médica, é abusiva a recusa.
- Súmula 95/TJSP. Havendo expressa indicação médica, não prevalece a negativa de cobertura do tratamento.
- Lei 12.880/2013. Quimioterapia oral (ambos os medicamentos) é cobertura obrigatória pelos planos.
A combinação dos nove pontos compõe tese juridicamente sólida e tecnicamente fundamentada, com alta probabilidade de êxito em sede de tutela de urgência (liminar) no foro do domicílio do paciente. A jurisprudência do medicamento irmão — olaparibe (Lynparza®), também inibidor PARP, com indicação consolidada em mCRPC — funciona como ancoragem analógica robusta enquanto a jurisprudência específica de talazoparibe se forma.
Reversão da negativa: NIP e liminar judicial
Em pacientes com mCRPC HRR-mutado, o tempo é crítico — cada mês sem tratamento adequado representa perda de chance terapêutica. A escolha entre via administrativa (NIP) e via judicial (liminar) depende do estágio clínico do paciente e da urgência do início do tratamento.
A NIP (Notificação de Intermediação Preliminar) é canal administrativo da ANS, gratuito e formal, com prazo de 5 dias úteis para resposta da operadora. Cria registro administrativo da recusa, fortalecendo eventual ação judicial. É indicada para paciente com prescrição médica completa e perfil molecular HRR documentado, doença com progressão controlada no momento (sem urgência vital imediata) e como primeira tentativa formal antes da via judicial. Em câncer de próstata avançado, contudo, em parte expressiva dos casos a NIP é indeferida e o caminho efetivo é a tutela de urgência.
A liminar judicial é a via direta. Em câncer de próstata metastático, o perigo de dano é evidente — cada semana sem tratamento adequado agrava o prognóstico. A tutela de urgência sai em 5 a 15 dias úteis em condições normais; em risco à vida (paciente com BRCA2, doença em progressão laboratorial ou em imagem), em 24 a 72 horas via plantão, com multa diária para descumprimento. A liminar é particularmente indicada quando a NIP foi indeferida ou não respondida no prazo, quando há progressão clínica ou laboratorial documentada (PSA em ascensão, novas lesões em imagem) ou quando a operadora recusa expressamente com fundamento em “fora do rol” ou “decisão da ANS”.
Documentação essencial antes do primeiro contato
Em câncer de próstata metastático com mutação HRR, a documentação organizada antecipa o ajuizamento e fortalece a fundamentação da tutela de urgência. Os itens abaixo devem ser reunidos antes da primeira consulta jurídica:
- Laudo anatomopatológico — diagnóstico histológico do adenocarcinoma de próstata com escore de Gleason e estadiamento patológico (TNM). Documento central da ação.
- Painel NGS / mutação HRR — resultado do painel molecular (tecido tumoral ou ctDNA) demonstrando mutação em BRCA1, BRCA2, ATM ou outro gene HRR. Justifica a indicação específica de PARP-inibidor.
- Estadiamento completo — PET-CT com PSMA (mais sensível em próstata), cintilografia óssea, ressonância de coluna ou pelve quando aplicável, marcadores tumorais (PSA seriado).
- Histórico de bloqueio androgênico — documentação da castração cirúrgica ou medicamentosa, e da progressão da doença sob bloqueio (definição de mCRPC).
- Prescrição do oncologista — receituário com indicação expressa de talazoparibe + enzalutamida, doses, ciclos e fundamentação clínica baseada em diretrizes NCCN/ESMO.
- Negativa por escrito — carta, e-mail ou protocolo da operadora com fundamentação da recusa. Sem documento formal, exigir formalização antes de ajuizar.
- Contrato do plano — íntegra do contrato com a segmentação contratada. Comprovantes de pagamento dos últimos 6 meses (adimplência).
- Cotações de mercado — valores do tratamento em hospitais e farmácias especializadas. Base para reembolso retroativo se houve custeio próprio durante o impasse.
Perguntas frequentes sobre a decisão da ANS e a cobertura
A ANS recusou a inclusão. O plano de saúde pode negar com fundamento na decisão de 24/04/2026?
Não. A decisão da ANS é administrativa e diz respeito à cobertura do Rol — não define a obrigação contratual da operadora frente ao paciente individual. Após a Lei 14.454/2022, o Rol é exemplificativo. A cobertura é obrigatória se satisfeitos os critérios objetivos do §13 do art. 10 da Lei 9.656/98 (eficácia comprovada, aprovação por agências de renome internacional, recomendação por órgãos de avaliação técnica). Os três estão satisfeitos pela combinação Talzenna + Xtandi.
Quanto tempo leva para conseguir uma liminar contra o plano nesse caso?
Em casos oncológicos com documentação completa (laudo, painel HRR, prescrição, negativa), o prazo típico é de 24 a 72 horas úteis no foro do domicílio do paciente. Em comarcas com despacho ágil, há registros de decisão em poucas horas via plantão. O fator determinante é a qualidade da prescrição médica e do painel molecular.
Qual o custo aproximado da combinação no Brasil?
O custo varia conforme a dosagem prescrita e a duração do tratamento. Em valores de mercado de 2026, a combinação representa aproximadamente R$ 35.000 a R$ 50.000 por mês de tratamento, considerando ambos os medicamentos. Como o tratamento pode durar 18-36 meses ou mais em pacientes respondedores, o custo total justifica plenamente a judicialização.
Sou paciente sem mutação HRR. Tenho direito à combinação?
Os dados do TALAPRO-2 mostram benefício também em pacientes não selecionados (ganho de ~9 meses de sobrevida vs. monoterapia), mas o benefício é maior em HRR-mutados (+14 meses). A indicação aprovada pela ANVISA é, atualmente, restrita ao perfil HRR-mutado. Para pacientes sem mutação HRR, a indicação seria off-label, exigindo fundamentação clínica mais robusta — mas a Súmula 102 do TJSP encerra os argumentos contra a cobertura off-label quando há prescrição médica fundamentada.
Posso pedir reembolso retroativo se já custeei o tratamento?
Sim. O reembolso retroativo é cabível quando o paciente custeou o tratamento por urgência clínica e necessidade imperiosa, demonstrando que a recusa da operadora foi indevida. A ação cumula obrigação de fazer (autorização para os ciclos futuros) e obrigação de pagar (reembolso dos valores já desembolsados, com correção monetária e juros).
O plano pode alegar que é “tratamento experimental” para negar?
Não. A combinação tem registro ANVISA, aprovações FDA e EMA, evidência publicada em revistas peer-reviewed e está incluída em diretrizes internacionais (NCCN categoria 1, ESMO, AUA). Não há nenhum elemento técnico que sustente a tese de “experimental”. A Súmula 102 do TJSP encerra esse argumento de modo definitivo quando há prescrição médica fundamentada.
O plano pode alegar custo desproporcional?
A jurisprudência majoritária do STJ e TJSP rejeita a tese de “custo desproporcional” como fundamento legítimo para negativa de tratamento oncológico. O AREsp 3.066.406 (Min. Marco Buzzi, fev/2026) consolida que medicamentos oncológicos estão fora do sistema do Rol — discussão sobre custo é juridicamente irrelevante em oncologia. O custo da terapia é elemento do contrato de plano de saúde, sendo obrigação da operadora prover a cobertura prevista em lei.
Há decisões judiciais específicas sobre Talzenna + Xtandi no Brasil?
Como a aprovação ANVISA e a decisão da ANS são recentes (2024-2026), a jurisprudência específica sobre essa combinação ainda está em formação. Contudo, há sólida jurisprudência sobre o medicamento da mesma classe — olaparibe (Lynparza) — em mCRPC, com ações majoritariamente julgadas procedentes em todos os tribunais estaduais. O fundamento jurídico é idêntico, o que permite ancorar a tese para Talzenna + Xtandi.
O painel NGS para identificar mutação HRR também tem cobertura obrigatória?
Sim. Quando há indicação médica para terapia-alvo dependente do perfil molecular, o painel NGS é parte integrante do tratamento e tem cobertura obrigatória pela operadora. A cobertura abrange tanto o painel em tecido tumoral quanto o painel em ctDNA (DNA tumoral circulante em sangue periférico) quando há indicação clínica específica.
Como o Belisário Maciel Advogados pode ajudar
Belisário Maciel Advogados atua exclusivamente em Direito Médico e da Saúde, com cluster oncológico aprofundado e responsabilidade técnica do sócio Dr. Luiggi Gustavo Maciel Giovannini (OAB/SP 513.090). A consulta inicial é dedicada a entender o caso, analisar a documentação clínica e jurídica, estimar o prazo realista de tutela de urgência e explicar honorários em contrato escrito. Atendimento presencial em Itaim Bibi (São Paulo) e digital em todo o Brasil, com plantão para urgência oncológica.
Para o panorama estratégico mais amplo, vale ler em paralelo o pilar Plano de Saúde, Câncer e Oncologia e os hubs 10 direitos do paciente oncológico e negativa de plano de saúde — caminhos da reversão. A análise específica do PARP-inibidor irmão está em Lynparza (olaparibe) — cobertura pelo plano de saúde.